SESSION de Décembre 2001
DEUG STPI - Première année - U.E.2 - "Réaction chimique"
Exercice 1 :
C = 3 108 m.s-1 - h = 6,62 10-34 J.s - e = 1,6 10-19 C - E0 = 13,6 eV = 2,18 10-18 J
Le spectre de l'atome d'hydrogène comporte une raie violette correspondant à une longueur d'onde de 411 nm.
Séries de raies pour l'atome d'Hydrogène :
n |
1 |
2 |
3 |
4 |
Nom |
Lyman |
Balmer |
Paschen |
Bracket |
Domaine spectral |
U.V |
Visible |
I.R |
I.R |
1) A quelle série appartient cette raie ?
2) Calculer sa fréquence et son énergie.
3) A quelle transition électronique n à p cette raie est-elle associée?
Exercice 2 : MPb= 207,2 g.mol-1 - MCl = 35,5 g.mol-1
Soit la réaction : Pb2+ (aq) + 2 Cl- (aq) = PbCl2 (s)
Pour déterminer la constante KR de cette réaction de précipitation du chlorure de plomb on procède a deux expériences différentes :
Expérience 1 : On introduit dans un bécher 20 mL d'une solution d'acétate de plomb (Pb2+ ; 2 CH3COO-) de concentration molaire 0,1 mol.L-1 et 20 mL de solution de chlorure de sodium ( Na+ ; Cl-) de concentration molaire 0,2 mol.L-1. On laisse la réaction se faire puis on filtre le contenu du bécher de manière à récupérer le solide formé. Après lavage et séchage du solide on pèse celui-ci et on trouve une masse de précipité de PbCl2 (s) : m = 0,3811 g. Calculer KR.
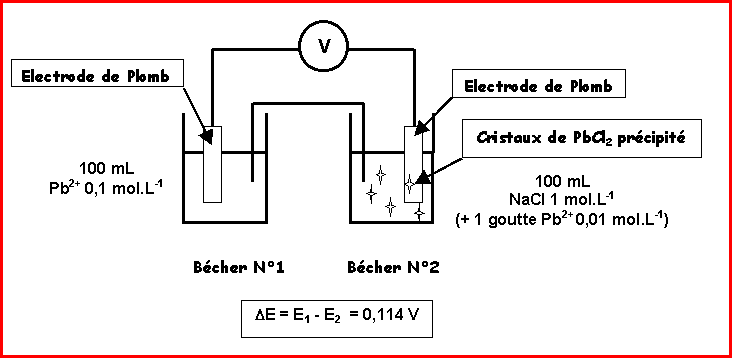
Expérience 2 :
On réalise la pile suivante (voir schéma)

a) Exprimer le potentiel de l'électrode 1 sachant que le couple d'oxydoréduction est le couple
Pb2+(aq) / Pb(s).
b) Exprimer le potentiel de l'électrode 2 sachant que le couple d'oxydoréduction est le couple
Pb2+(aq) / Pb(s).
c) Exprimer la différence de potentiel de la pile DE = E1 - E2
d) Sachant que DE = E1 - E2 = 0,174 V, calculer la concentration de l'ion Pb2+ dans le bécher N°2.
e) En supposant que la concentration des ions Cl- dans le bécher N°2 n'a pas été modifiée par l'ajout de Pb2+, calculer KR.
Exercice 3 :
Fe3+ / Fe : E01 = 0,77 V - HNO3 / NO(g) : E02 = 1,05 V
R = 8,31 J.K-1.mol-1 - 1 bar = 105 Pa - MFe = 56 g.mol-1
Le fer est oxydé en ions ferriques Fe3+ par l'acide nitrique concentré HNO3 qui est lui même réduit en monoxyde d'azote NO (composé gazeux).
1) Ecrire et équilibrer la réaction.
2) Calculer sa constante d'équilibre. Conclusion ?
3) On attaque 20 g de fer en poudre par un large excès de HNO3. Quel volume de gaz NO pourra-t-on recueillir sous 1,5 bar à 35°C ?
Exercice 4 : On à demandé à deux étudiants de représenter la classification périodique des éléments, voici le résultat de leur réflexion.
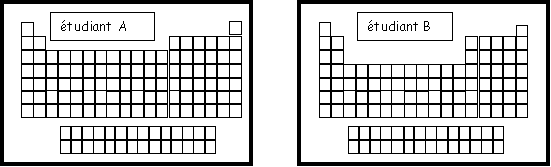
On demande de corriger leur(s) éventuelle(s) erreur(s) en justifiant simplement la réponse.
Etudiant A :
Etudiant B :