Exercice 1 :
Pour l’atome de Carbone et l’atome d’Hydrogène
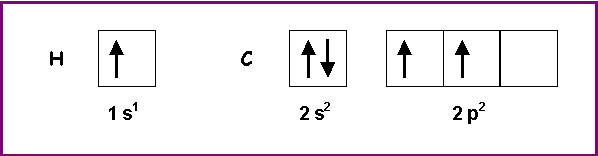
H : Z = 1 - 1 s1
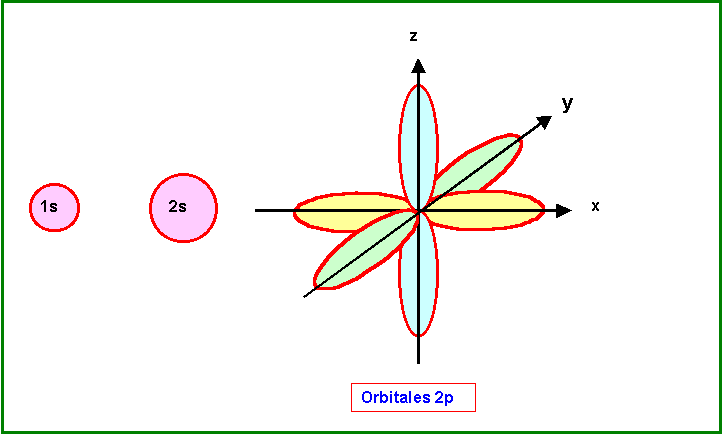
C : Z = 6 - 1 s1 2 s2 2 p2

- Quel composé devrait se former entre ces deux atomes si on considérait simplement le recouvrement de leurs orbitales atomiques de valence dans leur état fondamental?
Le Carbone est divalent et l'Hydrogène monovalent, il devrait donc se former le composé de formule CH2
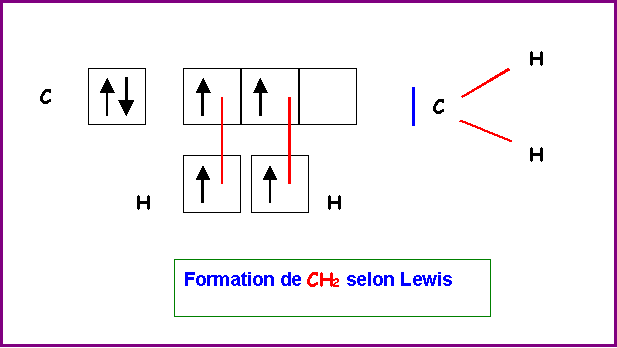
En réalité ce composé est très instable et n’existe pas à l'état naturel.
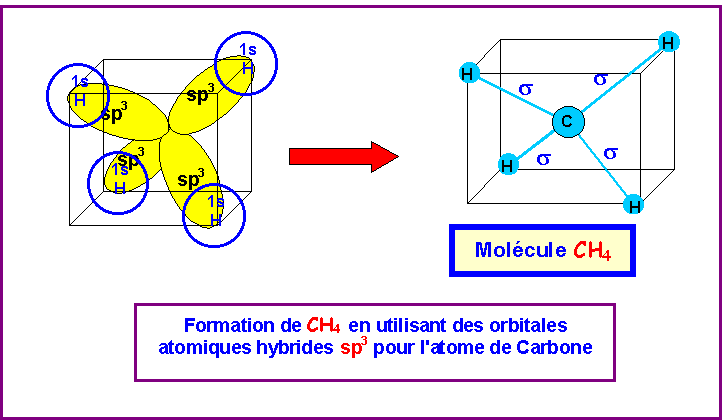
Le composé naturel le plus simple entre ces deux atomes est le méthane de formule CH4.
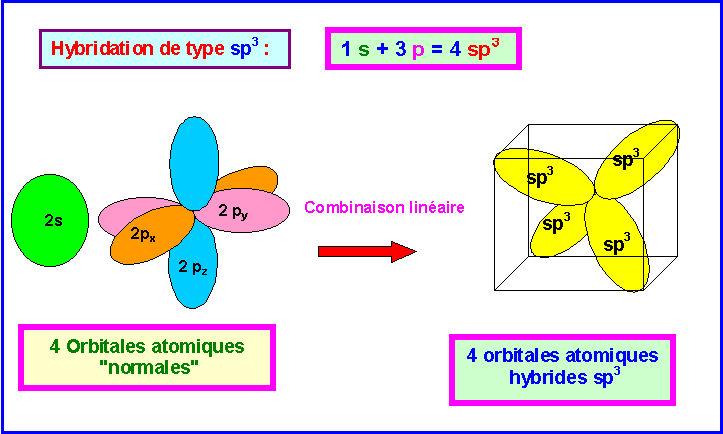
On peut utiliser l'état excité 2 s2 - 2 p2 de l'atome de Carbone pour augmenter sa valence et former quatre liaisons avec quatre atomes d'Hydrogène.
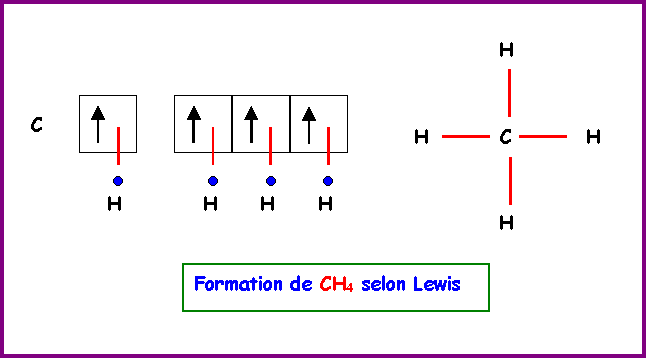
Les recouvrements se font de la manière suivante :
1) Orbitale 2 s de C / Orbitale 1 s de H :
Recouvrement axial - Liaison de type s
Les deux orbitales utilisées étant toutes deux de symétrie sphérique, la liaison C-H ainsi formée peut être orientée de façon tout a fait quelconque cette liaison n'a donc pas de direction particulière.
2) Orbitale 2 px de C / Orbitale 1 s de H :
Recouvrement axial - Liaison de type s
Pour obtenir un recouvrement maximal, la liaison C-H ainsi formée pointe dans la même direction que l'orbitale px.
3) Orbitale 2 py de C / Orbitale 1 s de H :
Recouvrement axial - Liaison de type s
Pour obtenir un recouvrement maximal, la liaison C-H ainsi formée pointe dans la même direction que l'orbitale py.
4) Orbitale 2 pz de C / Orbitale 1 s de H :
Recouvrement axial - Liaison de type s
Pour obtenir un recouvrement maximal, la liaison C-H ainsi formée pointe dans la même direction que l'orbitale pz.
On a donc finalement pour CH4 :
Une liaison "non dirigée" et trois liaisons pointant à angles droit dans les trois directions x,y,z.

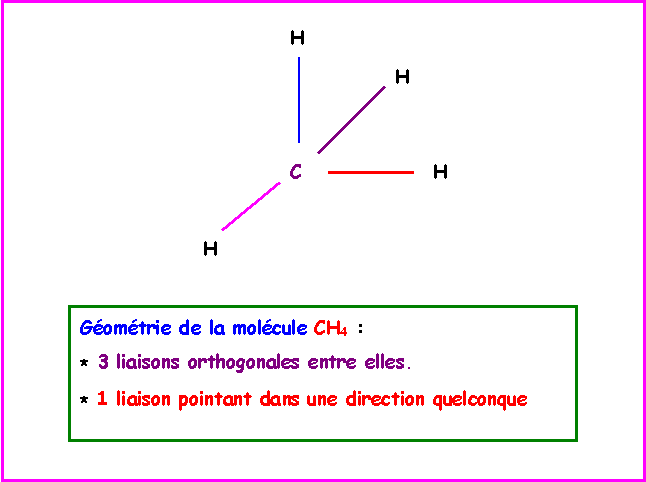
La géométrie réelle du Méthane est tétraédrique.
Cela peut être prévu par la méthode R.P.E.C.V ( ou V.S.E.P.R ou méthode de Gillespie) puisque la molécule est du type AX4.
L'hybridation conduisant à la géométrie tétraédrique ( AX4 ; AX3E ; AX2E2 ; AXE3 ) est l'hybridation de type sp3.